癫痫是一种常见的神经系统疾病,估计影响着全球6500万人。它以自发性癫痫反复发作为特征,主要由大脑内神经元活动的增强所驱动。在癫痫的多种类型中,颞叶癫痫(TLE)起源于颞叶的一个或多个解剖区域,是成人中最常见且对药物有抵抗性的癫痫形式。在某些情况下,仅切除杏仁核(杏仁核切除术)就足以消除癫痫发作。杏仁核复合体结构多样,由超过10个核团组成,但负责癫痫发作的核团和环路仍未确定。
2024年10月31日,浙江大学脑科学与脑医学学院、双脑中心李晓明/陈家东团队在Advanced Science杂志发表了题为“Posterior Basolateral Amygdala is a Critical Amygdaloid Area for Temporal Lobe Epilepsy”的研究论文,该研究揭示了后基底外侧杏仁核(pBLA)谷氨酸能神经元在癫痫发生和传播中的神经环路,并在TLE小鼠模型中确定pBLA是调节癫痫发作的杏仁核复合体中的关键核团。

为了操控C57BL/6J小鼠中pBLA的谷氨酸能神经元,研究人员使用了CaMKIIα启动子介导的腺相关病毒(AAV)工具。在小鼠的pBLA注射了AAV-CaMKIIα-ChR2-mCherry或AAV-CaMKIIα-mCherry的AAV,并在两侧植入光纤以光遗传学方式刺激pBLA中的谷氨酸能神经元(图1A)。脑电图(EEG)记录显示,光遗传学激活pBLA谷氨酸能神经元引起了持续39.75±5.31秒(n=6只小鼠)的显著癫痫样放电(图1D),显著增加了五种不同频率脑波的功率:δ波(0.5-4 Hz)、θ波(4-8 Hz)、α波(8-12 Hz)、β波(12-30 Hz)和γ波(30-500 Hz)(图1E)。这种激活还导致了5-6级癫痫发作(图1F),并引发了其他癫痫症状,包括瞳孔扩大和口吐白沫。值得注意的是,pBLA谷氨酸能神经元的短暂30秒激活可能导致动物突然死亡(癫痫阶段6;六只小鼠中有三只)。相比之下,光遗传学激活前基底外侧杏仁核(aBLA)的谷氨酸能神经元并未引起癫痫发作。
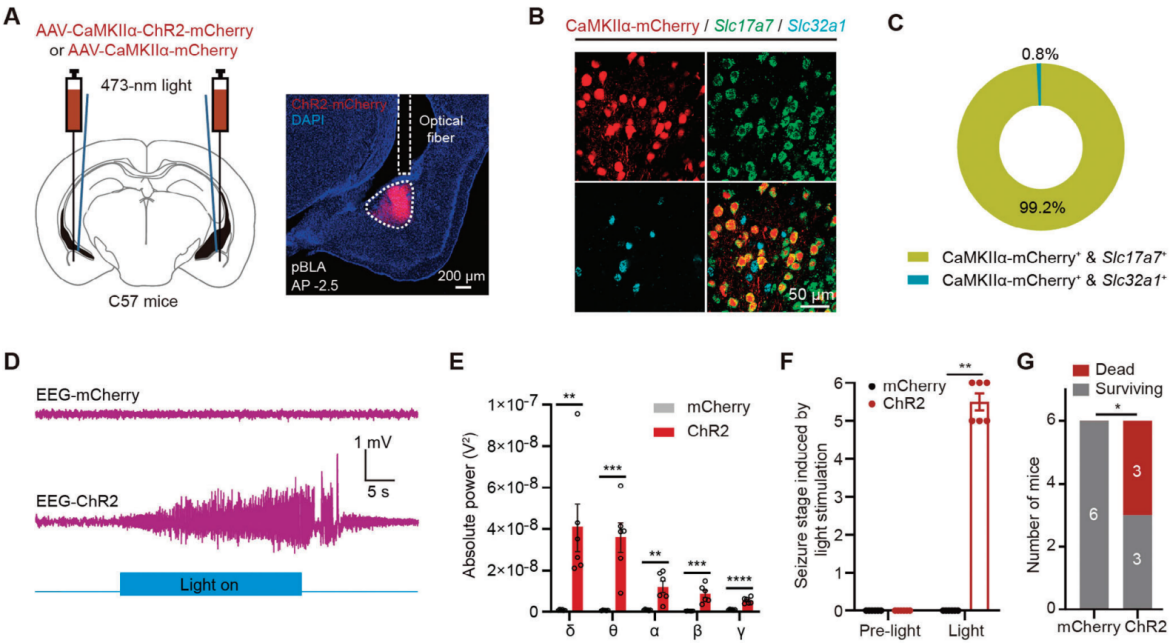
图1 光遗传激活pBLA谷氨酸能神经元可诱发癫痫症状甚至死亡
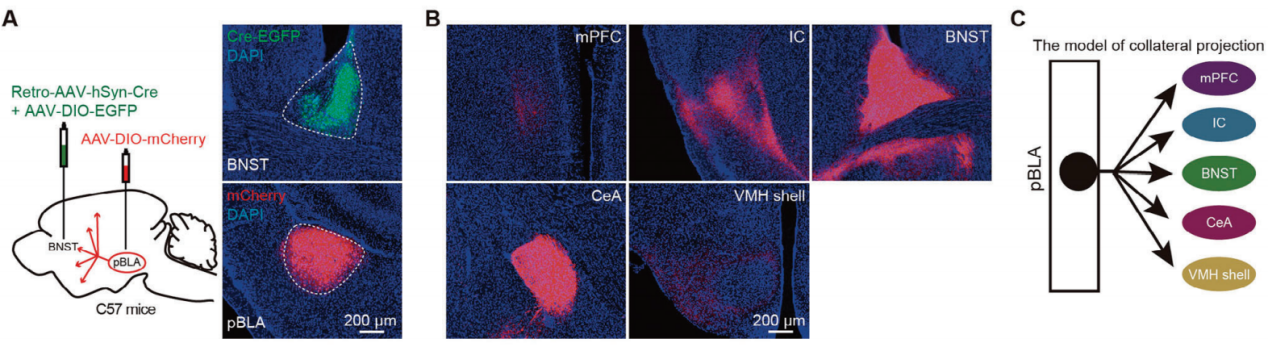
图2 用AAV逆行标记pBLA投射神经元
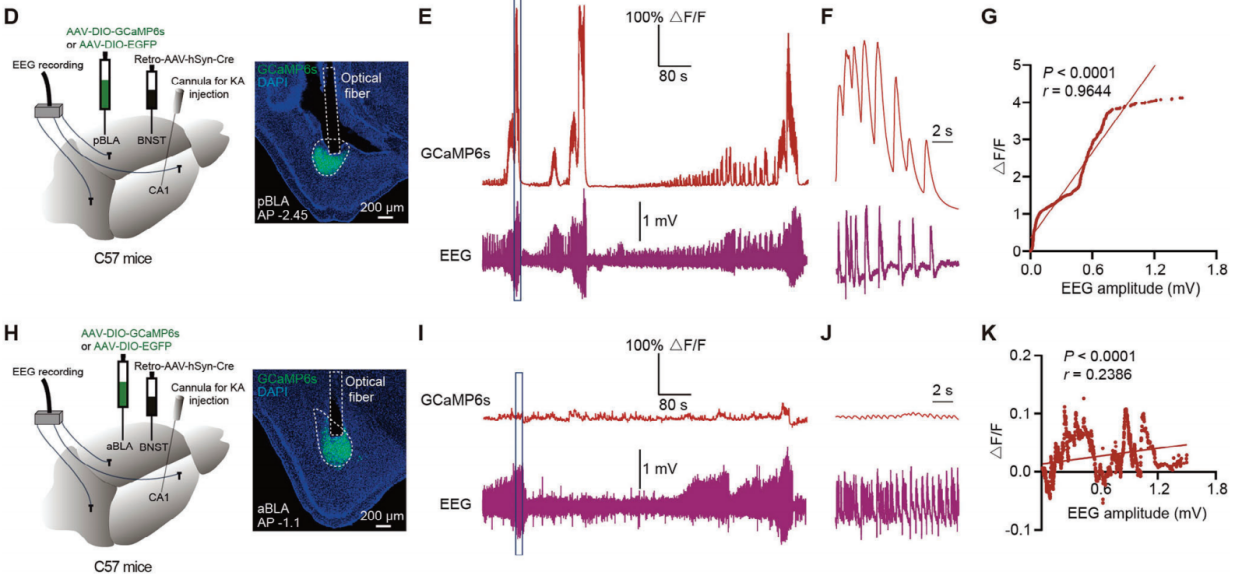
图3 侧支投射的pBLA神经元钙信号与癫痫发作活动同步
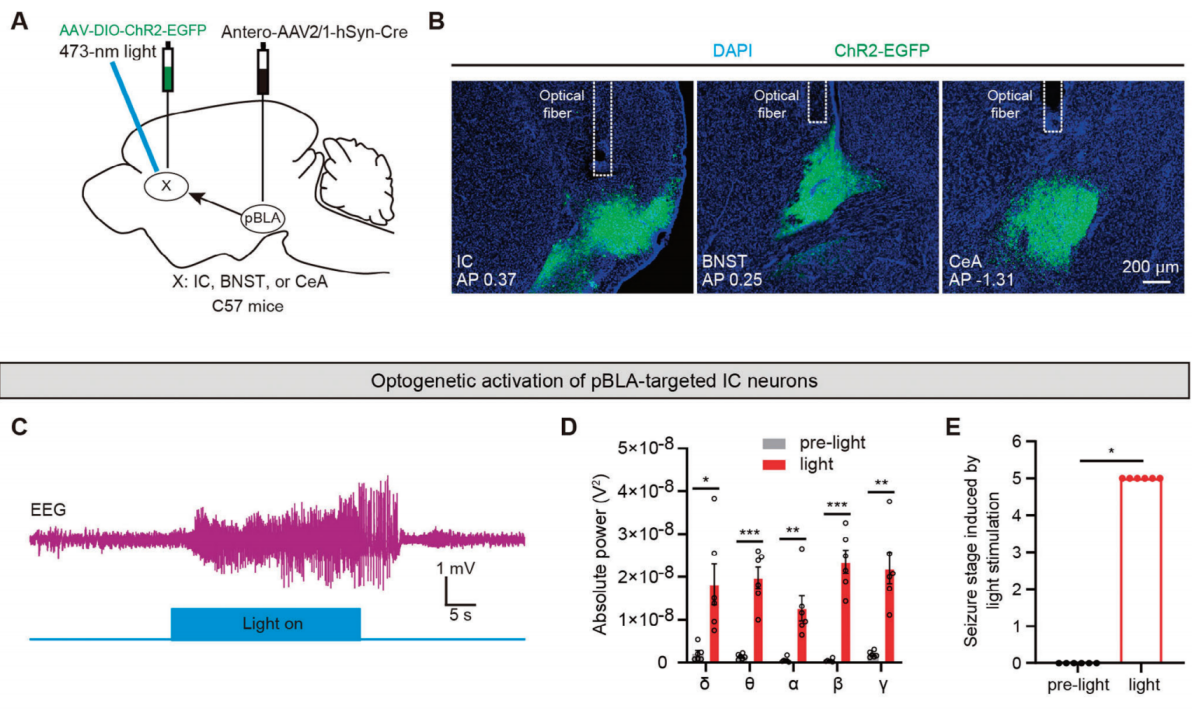
图4 光遗传激活靶向IC的pBLA神经元可诱发癫痫样放电和癫痫发作
为了进一步确定BNST GABA+或CeA GABA+神经元与pBLA谷氨酸能神经元之间的突触连接性质,研究人员进行了全细胞膜片钳电生理记录实验(图5D,K),结果显示光刺激从BNST或CeA投射到pBLA的轴突末梢时,在超过70%的mCherry标记的pBLA谷氨酸能神经元中诱发了抑制性突触后电流(eIPSCs),而不是兴奋性突触后电流(eEPSCs)(图5E,G,L,N)。此外,光遗传学激活pBLA谷氨酸能神经元对BNST GABA+或CeA GABA+投射的轴突末梢,结果显示表现出单突触抑制反应,记录到的eIPSCs被电压门控钠通道阻断剂河豚毒素(TTX, 1μM)阻断,随后被钾通道阻断剂4-氨基吡啶(4-AP, 100μM)恢复,并且被GABAA受体拮抗剂匹可毒素(PTX, 100μM)消除(图5E,F,L,M),结合病毒示踪、FISH和膜片钳电生理记录的结果,BNST GABA+或CeA GABA+神经元对pBLA谷氨酸能神经元形成了反馈抑制(图5B,C,I,J)。
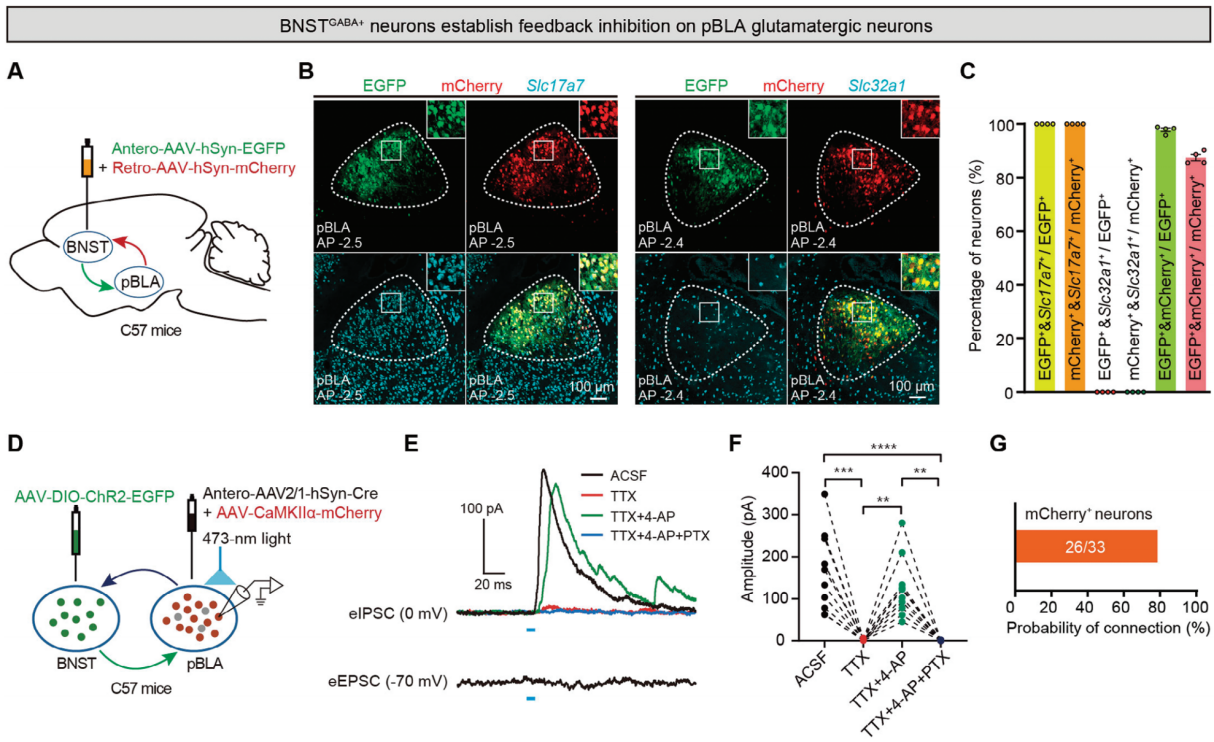
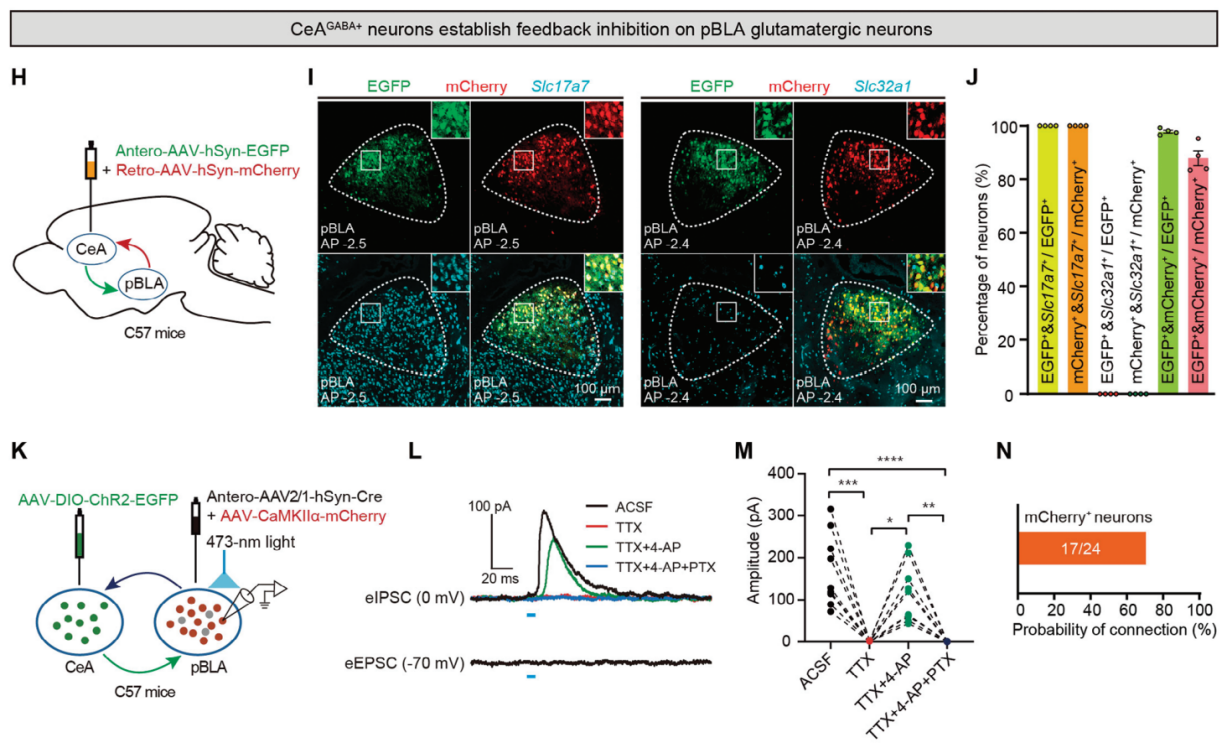
图5 BNST GABA+和CeA GABA+神经元对pBLA谷氨酸能神经元形成反馈抑制
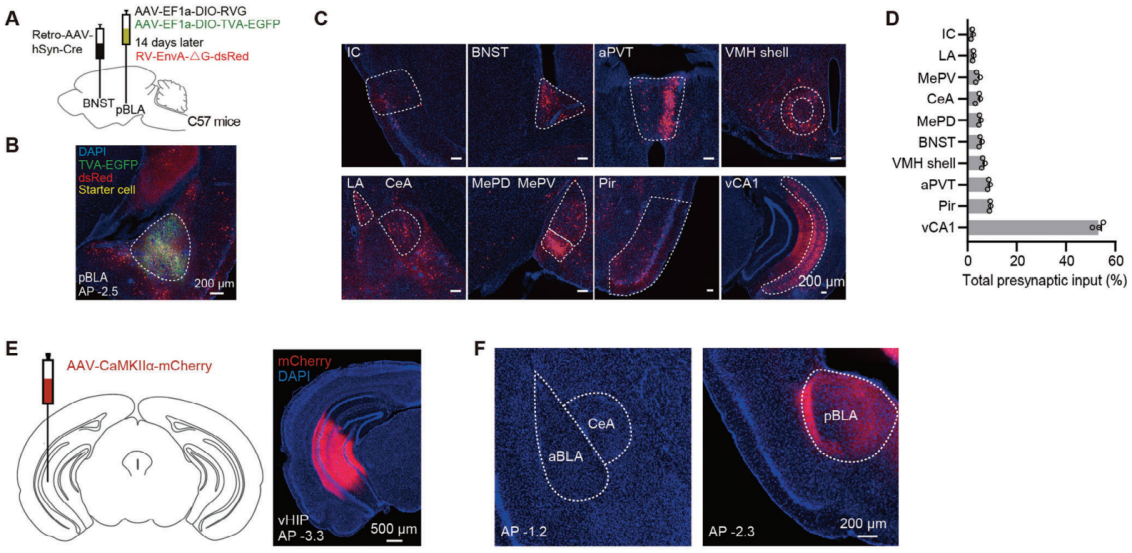
图6 从pBLA神经元投射到BNST的单突触逆行追踪
为了测试激活vCA1-pBLA神经环路是否足以引发癫痫发作,研究人员在C57BL/6J小鼠的vCA1注入AAV-CaMKIIα-ChR2-mCherry或AAV-CaMKIIα-mCherry,并在pBLA上方植入光纤。光遗传学激活vCA1-pBLA神经环路引发了癫痫样放电和癫痫行为。相比之下,尽管pBLA神经元也接收来自梨状皮质(Pir)和丘脑室旁核前部(aPVT)的突触输入(图7G),光遗传学激活兴奋性的Pir-pBLA或aPVT-pBLA神经环路路并未引发癫痫样放电或癫痫行为(图7H-J)。
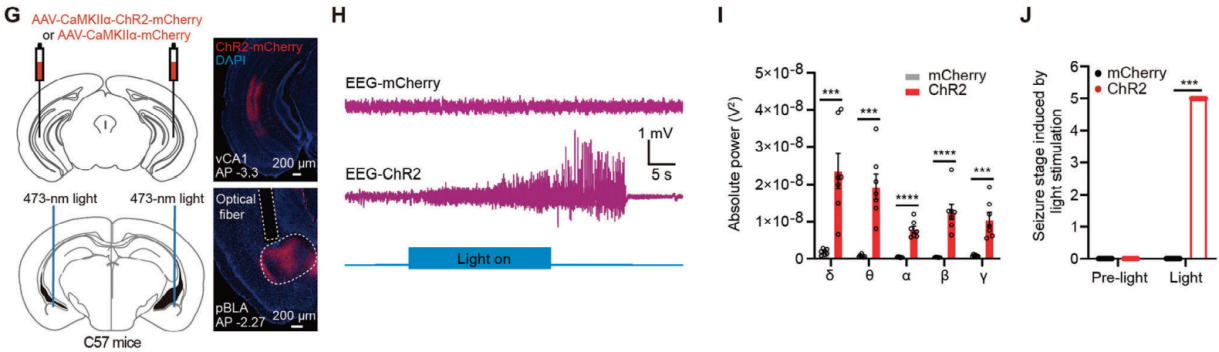
图7 光遗传激活vCA1-pBLA环路
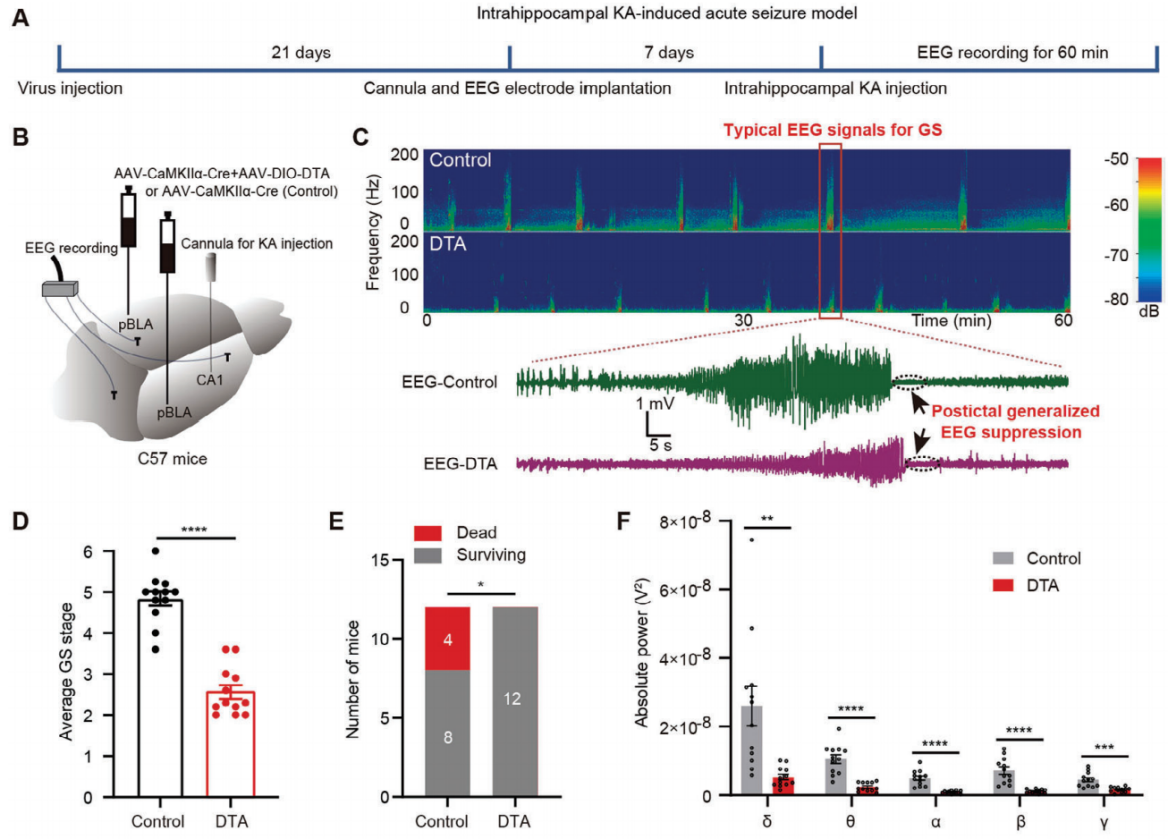
图8 消融pBLA谷氨酸能神经元可以抑制KA诱导的急性癫痫发作
接下来,研究人员探索了消融pBLA谷氨酸能神经元是否能够抑制KA诱导的慢性自发性癫痫发作。在海马注射KA,双侧引入AAV-DIO-DTA和AAV-CaMKIIα-Cre进行pBLA神经元消融,并在颅骨表面放置电极进行EEG记录。在KA注射后七周,每天观察超过8小时对小鼠进行评估,连续5天评估自发性高电压尖峰(> 0.5 mV)(图9G)。消融pBLA谷氨酸能神经元显著减少了自发性高电压尖峰的数量(图9H,I)。在pBLA消融的小鼠中也未观察到GSs(图9J,K)。这些发现表明,消融pBLA神经元有效地减轻了慢性TLE模型中的癫痫发作。
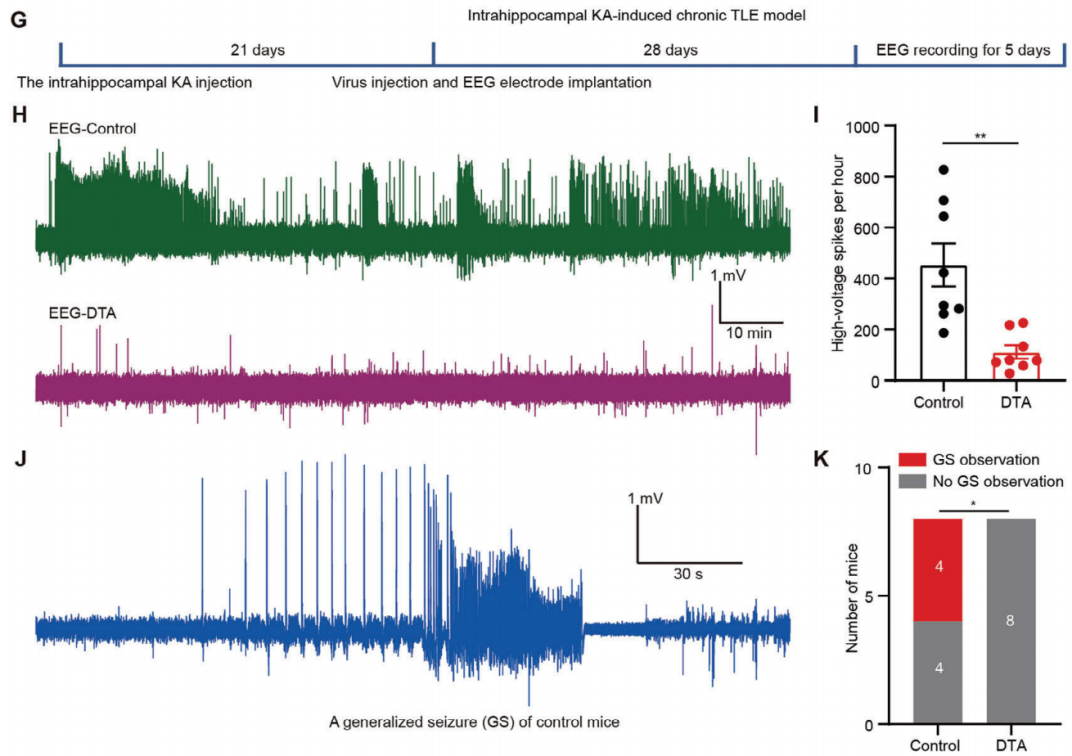
图9 pBLA神经元消融减轻慢性TLE模型中的癫痫发作
本文未经授权禁止转载
如有需要,可联系小编获取原文