基因表达(gene expression)是指将来自基因的遗传信息合成功能性基因产物的过程。基因表达产物通常是蛋白质,但是非蛋白质编码基因如转移RNA(tRNA)或小核RNA(snRNA)基因的表达产物是功能性RNA。
基因过表达(gene overexpression)是将目的基因编码区序列(CDS)克隆到相应的质粒或病毒载体上,利用载体骨架上构建的调控元件,使基因可以在人为控制的条件下实现大量转录和翻译,从而实现目的基因的过表达。此外,还可选择报告基因进行示踪或抗性基因进行筛选。
常用的病毒载体有腺相关病毒载体、慢病毒载体、腺病毒载体和逆转录病毒载体等,广泛应用于体外和体内基因功能研究。
根据实验需求、目的基因和用途不同,选择不同的载体。
| 腺病毒 | 慢病毒 | 逆转录病毒 | 腺相关病毒 | |
| 直径范围 | 60-90 nm | 90-110 nm | 90-100 nm | 20-30 nm |
| 复制类型 | 自主 | 无 | 无 | 无 |
| 基因容量※ | 5~6 kb | 4 kb | 1.6 kb | 2.5 kb |
| 整合机制 | 非整合 | 随机高频 | 随机高频 | 定向低频 |
| 细胞感染 | 类型广泛 | 类型广泛 | 分裂细胞 | 血清型决定 |
| 滴度范围 | 1011~12 pfu/ml | 108~9 tu/ml | 107~8 tu/ml | 1012~13 vg/ml |
| 体外感染 | 可用 | 推荐 | 可用 | 可用 |
| 定位注射 | 可用 | 可用 | 推荐 | 推荐 |
| 病毒种类 | 起始时间 | 持续时间 | 滴度要求 | 扩散能力 | 免疫原性 | 细胞类型 |
| 腺病毒 | 2-3天 | <10天 | >1X1010 | 强 | 强 | 广泛 |
| 慢病毒 | 3-4天 | >2个月 | >1X108 | 一般 | 一般 | 广泛 |
| 逆转录病毒 | 3-4天 | >2个月 | >1X107~8 | 一般 | 一般 | 分裂细胞 |
| 腺相关病毒 | 2-3周 | >3个月 | >1X1012 | 强 | 弱 | 血清型决定 |
| 元件名称 | 名称 | 用途 |
| 启动子 | CMV、EF1a、hSyn、TRE3g等、 | 广谱性、组织特异性和诱导型启动子启动转录 |
| 常用标签 | GFP、EGFP、YFP、mCherry、DsRed2、tdTomato、BFP-tag、CFP等 | 荧光标签 |
| His、flag、GST、HA、Myc等 | 亲和标签 | |
| 增强子 | WPRE、SV40等 | 加强基因转录 |
| 抗性基因 | KanR、AmpR等 | 原核细胞抗性筛选 |
| PuroR、Neo、Diphtheria toxin、Actidione等 | 真核细胞抗性筛选 | |
| 连接元件 | 2A(T2A、P2A、E2A等)、IRES | 用来连接2个表达基因 |
常规的蛋白表达的同时可以为蛋白表达添加融合或非融合的荧光标签,亲和标签,亚细胞定位系列等一系列修饰。
举例图谱结构:
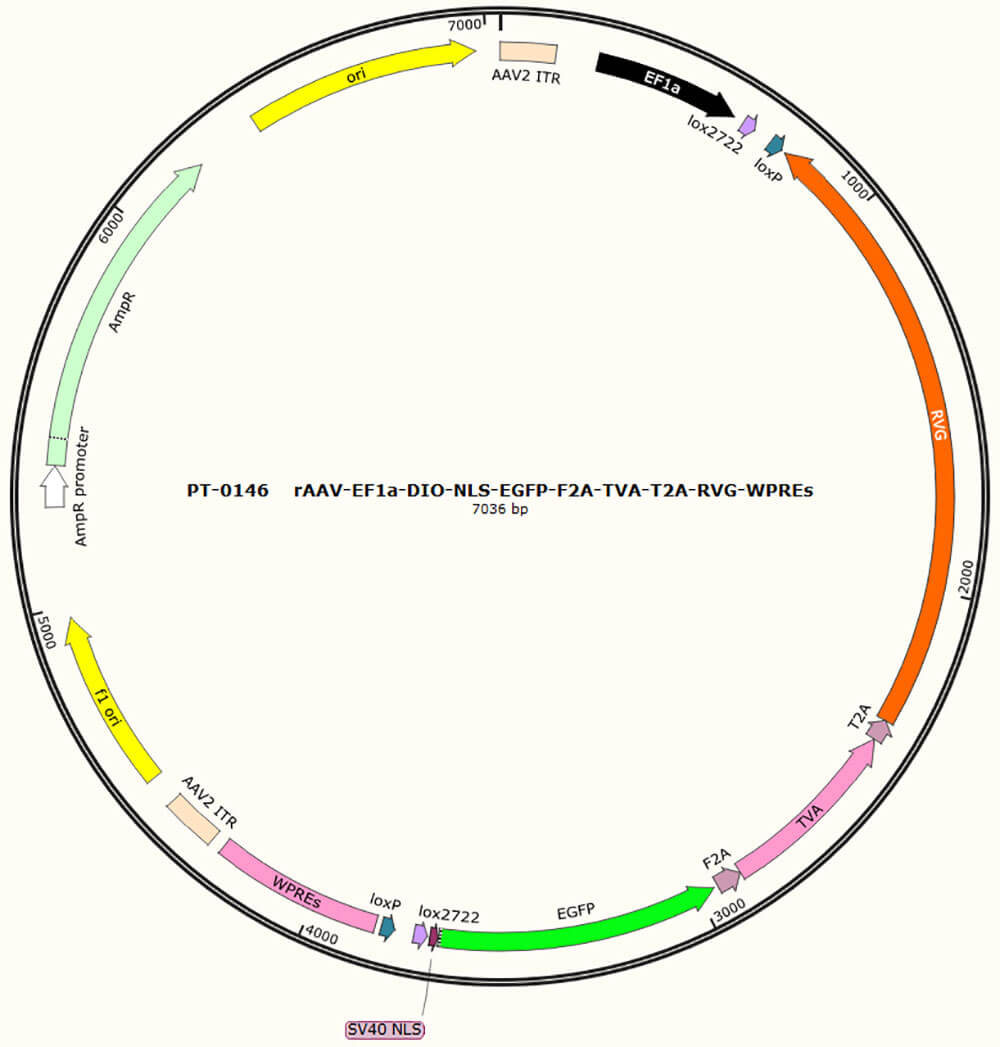
与常规蛋白表达不同的是,由于非编码RNA(链接非编码RNA介绍)仅仅转录但不翻译,无蛋白产生,因此此类表达载体(尤其是lncRNA)最好独立表达荧光蛋白,且常规蛋白表达的修饰基本不能使用。目前常见的非编码RNA主要为microRNA、lncRNA、circRNA三大类表达载体与之对应。
举例图谱结构:

细胞毒性蛋白表达与常规蛋白表达的载体除少量修饰外并无在明显区别,但在AAV载体制备过程中对表达的毒蛋白进行抑制才能产生。此载体主要用于过表达各种对细胞有毒害的蛋白。
举例图谱结构:
| 病毒载体类别 | 目的基因类型 | 编号 | 载体名称 |
| 腺相关病毒 | 编码基因 | BC-0012 | pAAV-EF1a-EGFP-WPRE-pA |
| circRNA | pAAV-ciR | ||
| lncRNA | pAAV-EF1a-lncRNA-pA-CMV-EGFP-pA | ||
| microRNA | |||
| 慢病毒 | 编码基因 | pLV-EF1a-EGFP-WPRE-pA | |
| circRNA | pLV-ciR | ||
| lncRNA | pLV-EF1a-lncRNA-CMV-mCherry-WPRE | ||
| microRNA |
1.MEN1(multiple endocrine neoplasia type 1)蛋白能够结合P35(Cdk5 regulatory subunit 1)启动子并促进P35表达。张杰课题组通过对MEN1缺陷小鼠注射AAV病毒(AAV2-CamKII-p35-T2A-GFP-WPRE)恢复p35的表达,发现增加了神经元树突的复杂性。
载体结构分析:CamKII启动子+ p35基因+自剪切2A肽+非融合GFP绿色荧光标签。
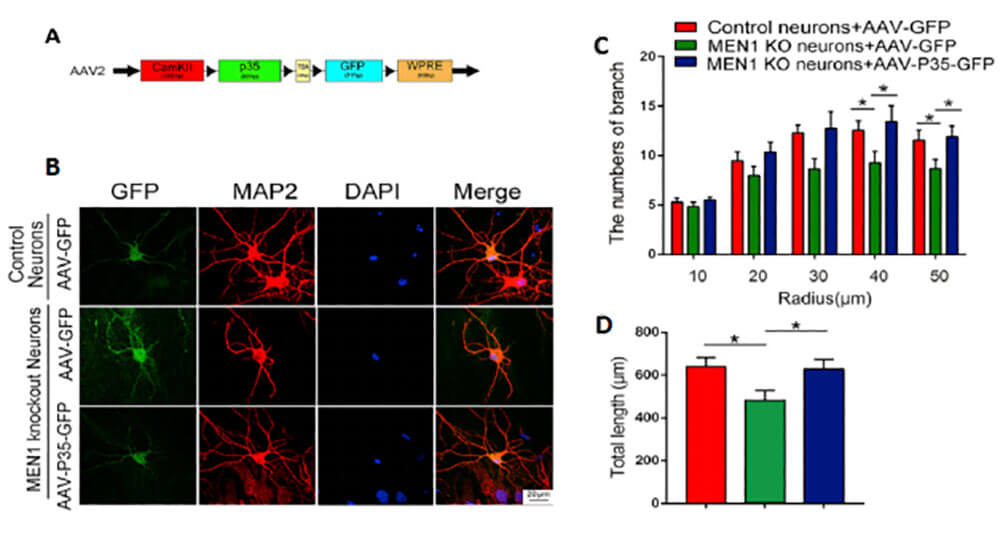
图1 对MEN1缺陷小鼠注射AAV2-过表达p35病毒可恢复p35的表达(图源:Zhuang, K.,et al., Cell reports, 2018)