客户高分文章
High impact factor articles from customers

三年聚变,共创辉煌。布林凯斯在神经科学领域持续稳步发展,以先进的科研技术和优秀的服务助力客户在Cell Research、Nature neuroscience、Neuron、Advanced Science、Nature Communications、Cell Reports等多家知名国际期刊上成功发表了大量文章。
小布精心整理了2024年第1个月,客户发表的6篇高分文章,并进行概要解读。此次收录的文章涵盖多个研究方向,涉及神经疾病、神经功能环路、神经分子机制等多个领域,快来和小布一起回顾下吧~
恐惧消退相关新机制
文章题目
Synapsin 2a/Synaptogyrin-3 interaction regulates fear extinction in mice (2024.01.04)
发表期刊
Journal of Clinical Investigation,IF:15.9
研究团队
华中科技大学同济医学院基础医学院刘丹教授、朱铃强教授团队
内容概要
该研究首次发现上调的突触蛋白Synapsin 2a (Syn2a)可通过其特定的H结构域结合Synaptogyrin-3(Syngr3)中的91-99氨基酸,从而导致IL-BLA中间能神经元环路的突触前抑制。透血脑屏障的穿膜肽或FDA批准的抗HIV药物利托那韦能够阻断Syn2a和Syngr3之间的相互作用,从而有效地改善恐惧记忆的消退,为PTSD的治疗提供了崭新的方向。
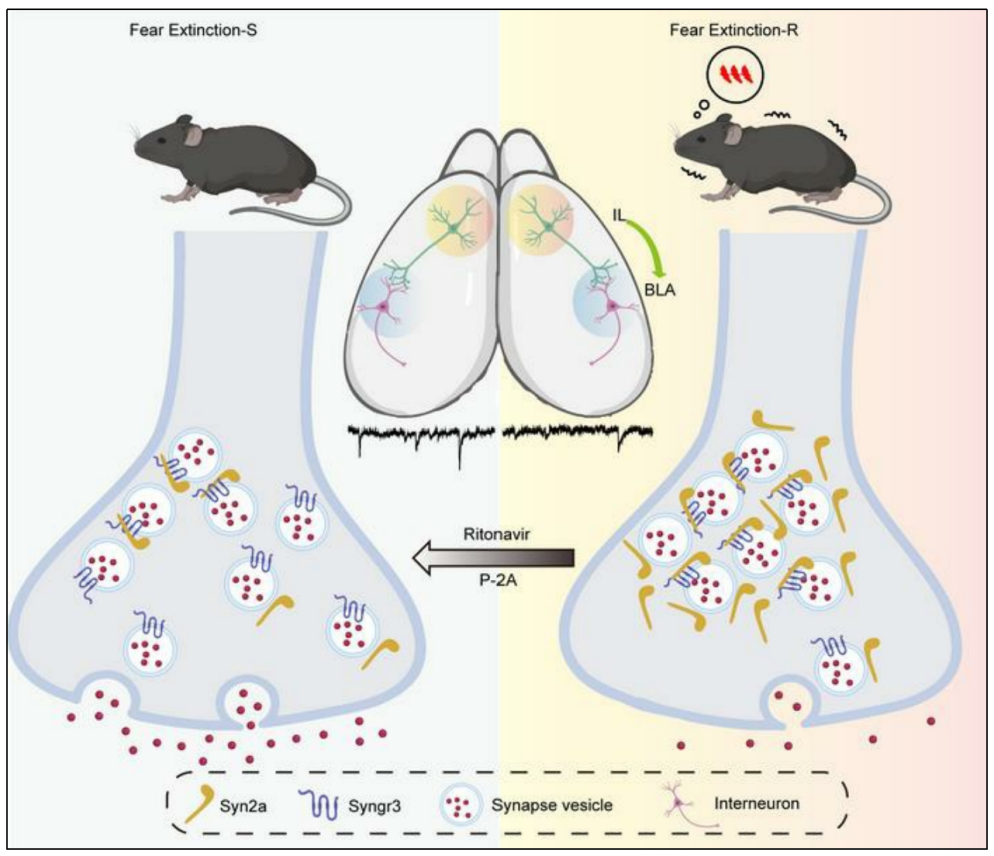
原文链接:https://www.jci.org/articles/view/172802
小胶质细胞介导焦虑消退
文章题目
Microglia govern the extinction of acute stress-induced anxiety-like behaviors in male mice (2024.01.10)
发表期刊
Nature Communications,IF:16.6
研究团队
中国科学技术大学张智教授团队
内容概要
该研究综合运用了在体多通道记录、三维重构技术和化学遗传学等,发现急性束缚应激导致小鼠中央杏仁核CeA中GABACeA能神经元的活性增加,导致12h内的焦虑样行为;同时,通过MST4-NF-κB-CX3CL1信号增加GABACeA神经元CX3CL1分泌,从而激活CeA中的小胶质细胞。活化的小胶质细胞反过来通过吞噬GABACeA神经元树突棘来抑制其活性,最终导致由束缚应激诱导的焦虑样行为的消失。综上,本研究阐释了小胶质细胞吞噬树突棘促进急性应激诱导的焦虑样行为的消失的分子机制。本文的发现拓宽了我们对小胶质细胞驱动的负反馈机制在保护大脑中作用的理解。而且本文发现急性应激早期的小胶质细胞激活可以在调节神经元活动中发挥保护作用,这与以往研究中的慢性应激的促伤害作用不同。
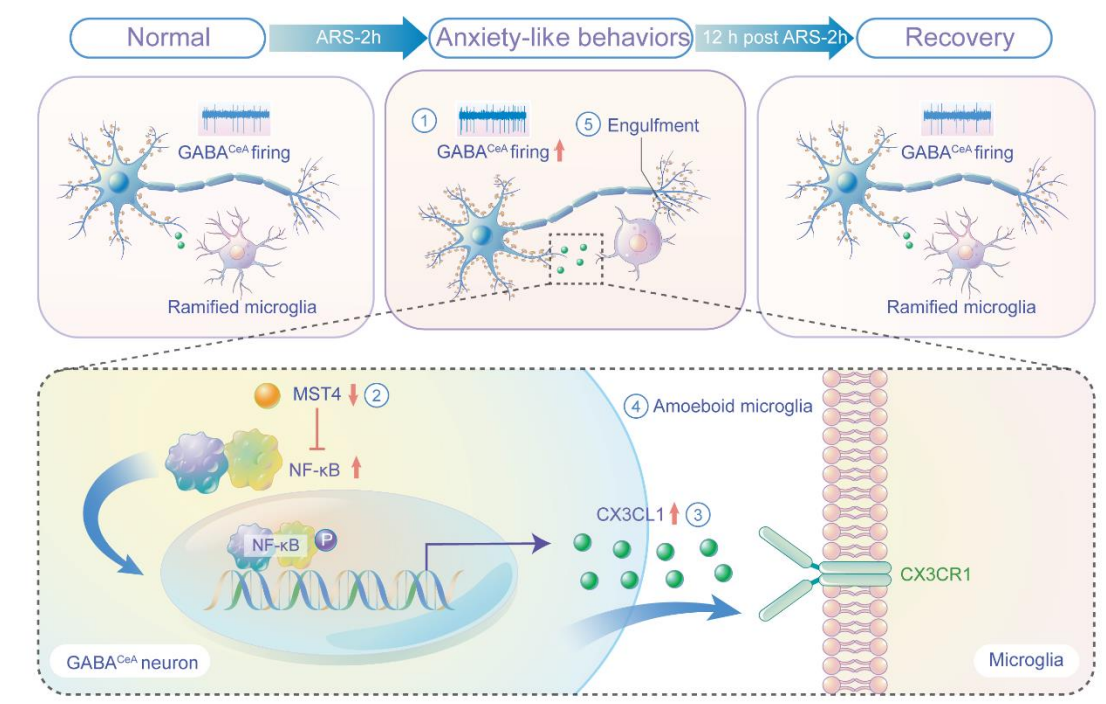
原文链接:https://www.nature.com/articles/s41467-024-44704-6
模拟神经环路闭环运行规律
文章题目
Dual electrical stimulation at spinal muscular interface reconstructs spinal sensorimotor circuits after spinal cord injury (2024.01.19)
发表期刊
Nature Communications,IF:16.6
研究团队
苏州大学神经科学研究所刘耀波教授团队
内容概要
研究人员比较了EEMS,EES和MS对感觉运动神经环路的结构和功能的促进作用,发现仅有在10-20Hz刺激频率条件下的EEMS可以有效恢复感觉运动神经环路的多突触电传导功能,以及后肢的运动功能。通过神经环路示踪,在体电生理记录和光纤记录,研究人员发现10-20Hz的EEMS重塑了脊髓感觉运动神经环路(运动神经元-肌肉间的连接,感觉神经元-运动神经元间的连接,中间神经元-运动神经元间的连接),增强了谷氨酸能神经元对运动神经元的支配。该研究建立了一种脊髓-肌肉界面的双重电刺激系统,模拟脊髓感觉运动神经环路的闭环运行规律,从而在结构和功能水平重建脊髓感觉运动神经环路,使人们对神经调控在神经环路重组中的作用有了更深入的了解,并为中枢神经损伤后的临床治疗提出了一个潜在的框架。
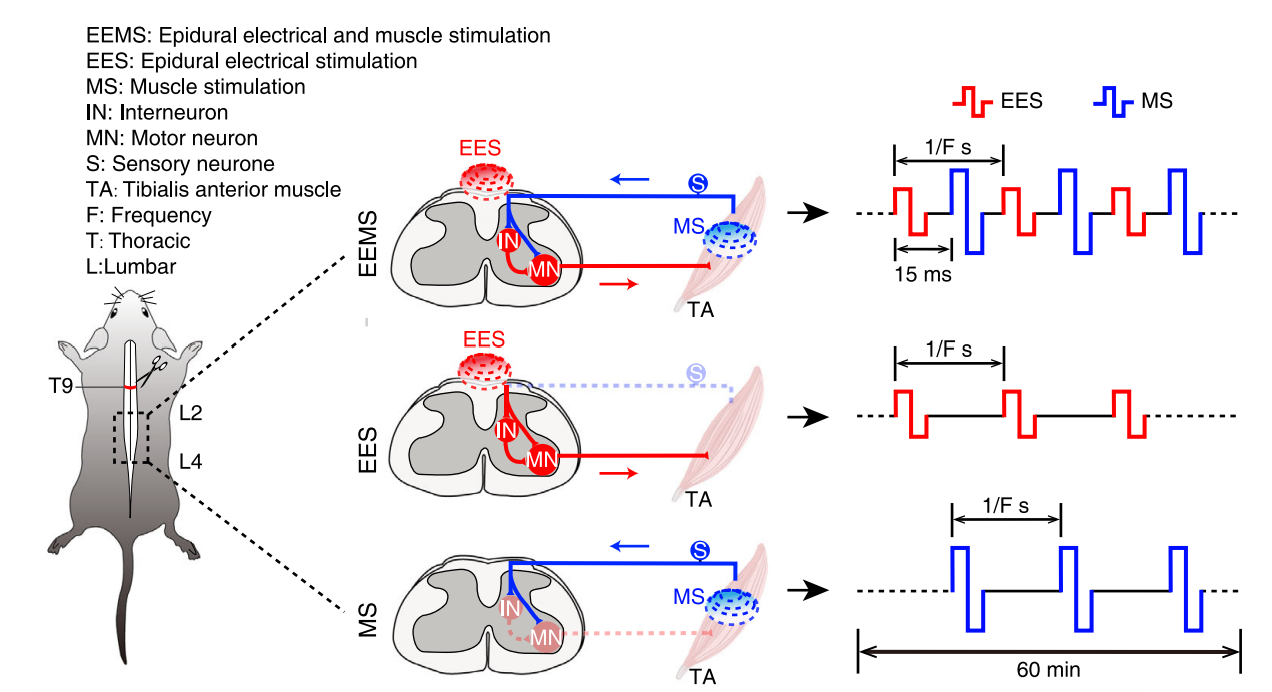
原文链接:https://www.nature.com/articles/s41467-024-44898-9
脑-脾调控疼痛介导免疫反应
文章题目
Somatosensory cortex and central amygdala regulate neuropathic pain-mediated peripheral immune response via vagal projections to the spleen (2024.01.30)
发表期刊
Nature Neuroscience,IF:25
研究团队
中国科学技术大学张智教授团队
内容概要
研究人员利用流式细胞术、神经示踪、钙成像技术、膜片钳电生理、光遗传学、化学遗传学等方法,发现脑脾轴调节不同慢性痛模型引起不同类免疫反应。S1HL与AChDMV-spleen形成兴奋性突触联系,促进SNI 1d小鼠TH2免疫反应;CeA与AChDMV-spleen形成抑制性突触联系,抑制SNI 4w小鼠TH2免疫反应。本篇文章发现疼痛介导脾脏TH2免疫反应受两条下行通路调控:一条为S1HL发起的谷氨酸能通路,另一条为CeA发起的GABA能通路,两条通路汇集于DMV乙酰胆碱能神经元,进而调节免疫反应。该研究首次揭示脑脾轴下行调控疼痛引起免疫反应,并阐释其细胞、环路机制,为神经免疫疾病的治疗提供论基础及药物靶点。
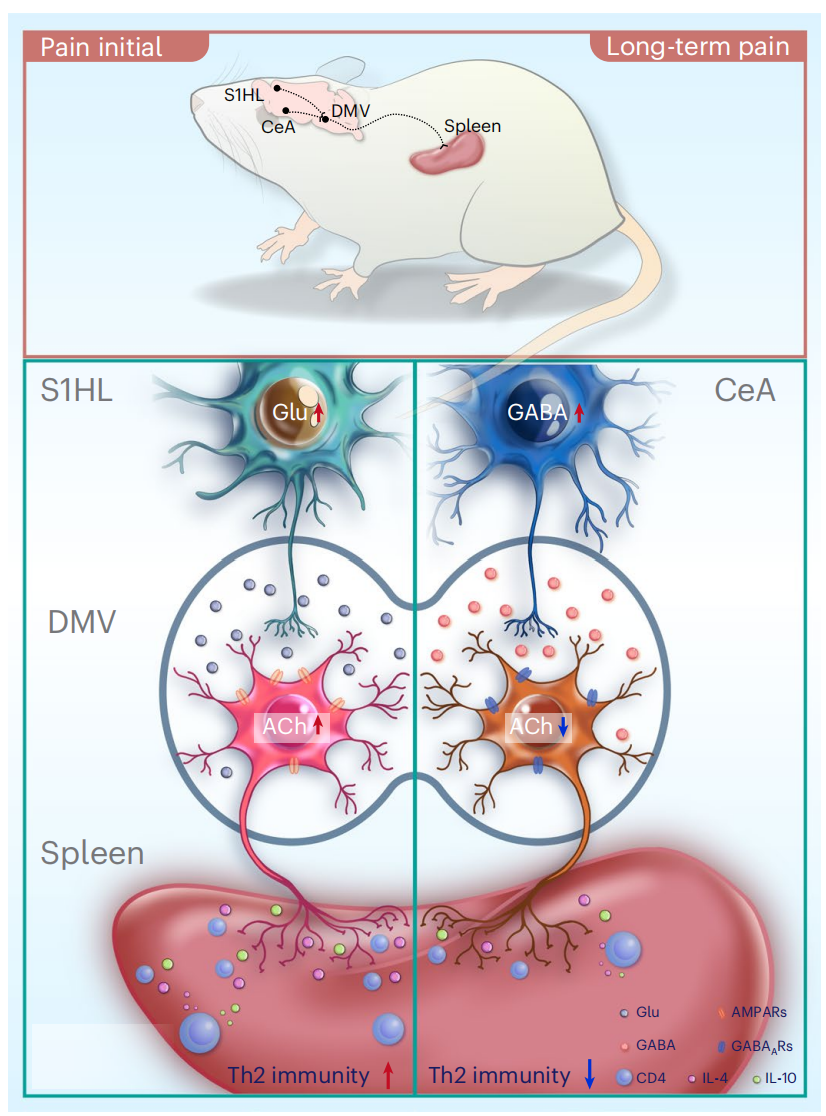
原文链接:https://www.nature.com/articles/s41593-023-01561-8
靶向小胶质细胞清除Aβ策略
文章题目
Clearance of b-amyloid and synapses by the optogenetic depolarization of microglia is complement selective (2024.01.31)
发表期刊
Neuron,IF:16.2
研究团队
中国科学院深圳先进技术研究院脑所詹阳研究员团队
内容概要
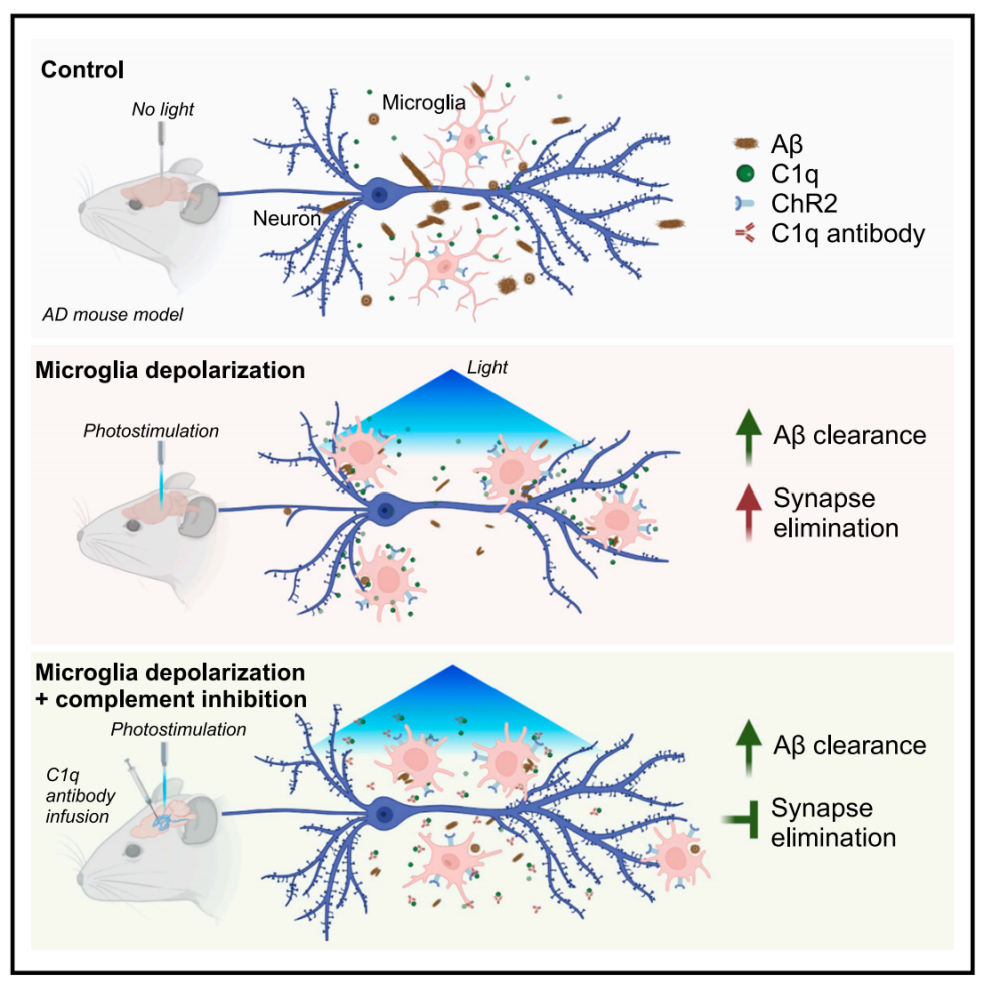
研究人员首先在离体方面成功将光感基因蛋白表达于小胶质细胞细胞系和原代细胞中,发现光遗传激活可以有效的使得细胞去极化,进而发现光刺激激活小胶质细胞后对Aβ以及突触小体等物质的吞噬能力增强。采用来自AD病人组织毒性更强的Aβ蛋白,研究团队也发现光激活小胶质细胞可以增强Aβ吞噬,发现光遗传激活小胶质细胞可以导致光照区域的细胞数量、形态发生明显变化。团队发现光遗传激活小胶质细胞导致神经突触丢失同时,补体通路分子C1q发生上调。进而团队通过抑制C1q,发现小胶质细胞光遗传激活不再吞噬神经突触。在AD模型中,发现C1q抑制后,光遗传激活小胶质细胞可以清除Aβ,但并不吞噬神经突触,进而实现Aβ清除同时而不杀伤神经突触。因而,本研究提供了一种靶向小胶质细胞的调控策略,该方法可以有效减少神经退行性疾病中的毒性蛋白聚集体,而同时保留正常突触连接。
原文链接:https://doi.org/10.1016/j.neuron.2023.12.003
运动改善焦虑神经环路机制
文章题目
A role for the cerebellum in motor-triggered alleviation of anxiety (2024.01.31)
发表期刊
Neuron,IF:16.2
研究团队
南京大学生命科学学院朱景宁教授团队
内容概要
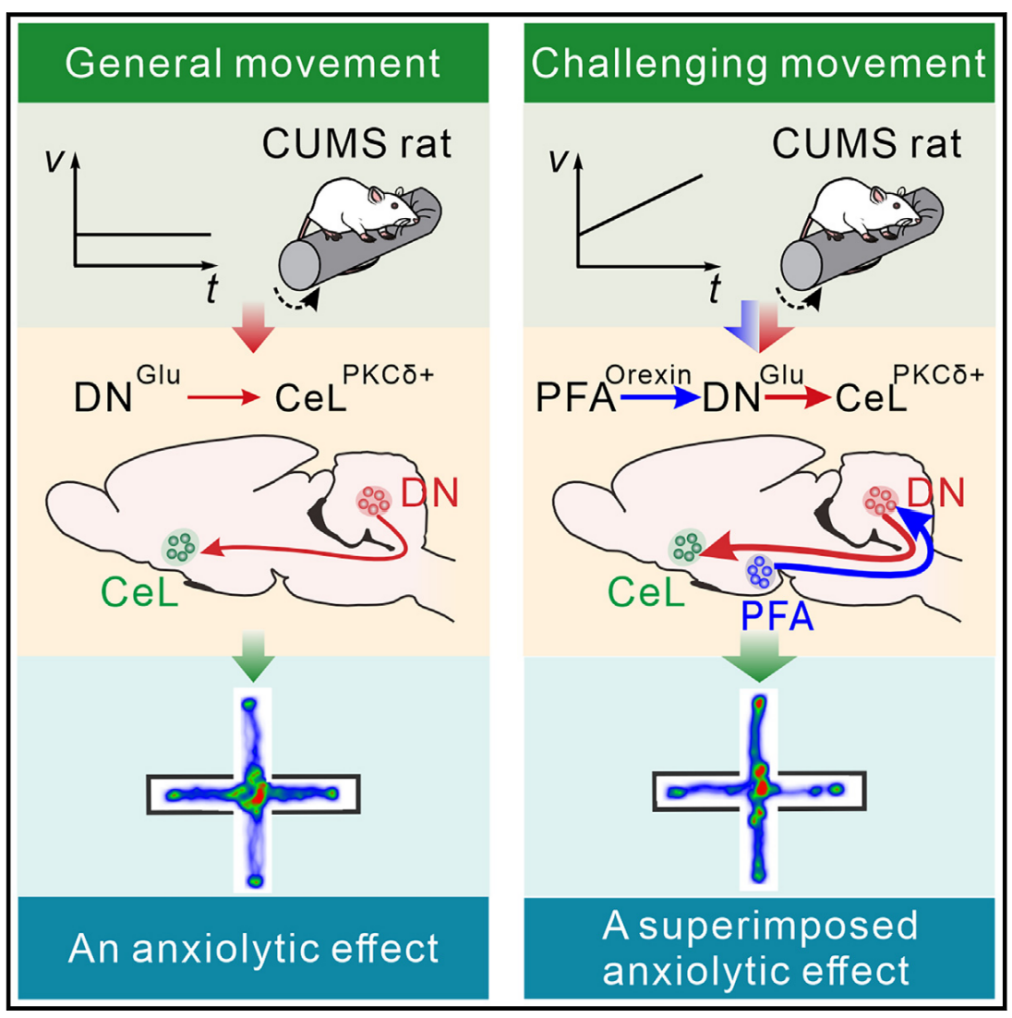
研究人员发现在orexin-cre大鼠下丘脑穹窿周区(PFA)中具有直接支配小脑DN的orexin能神经元,且这些神经元与直接支配杏仁核的orexin能神经元分属不同亚群,进一步兴奋和驱动DN-CeL投射,可以对慢性不可预知温和应激(CUMS)诱导的焦虑模型大鼠产生更强的抗焦虑效应。提示PFA-DN-CeL三元神经环路很可能像多档位变速箱和发动机一样工作,能够在两个强度水平上介导运动对焦虑的改善效应。运用静息态功能磁共振成像(fMRI)技术、离体脑片膜片钳结合光遗传学操控实验、在体光/化学遗传学技术、神经环路示踪技术,以及荧光显微光学切片断层成像技术( fMOST)等神经科学相关技术,在介观尺度上对DN-CeL神经元的直接长时程投射进行重构,在功能和结构上提示小脑与杏仁核之间存在相互作用并与焦虑相关。该项研究成果不仅有助于深入认识小脑的非运动功能,以及运动-情绪互作和机体躯体-非躯体反应整合的神经机制,而且有助于开发更为有效的运动处方,以及靶向小脑的侵入性和非侵入性干预策略,治疗焦虑等情绪情感障碍提供新思路。
原文链接:https://doi.org/10.1016/j.neuron.2024.01.007