创伤后应激障碍(PTSD)是一种难治性精神疾病,通常是由严重事故或灾难引起的。PTSD在全球范围内的终生患病率为1.9-6.8%,传统暴露治疗或药物治疗对40%的患者无明显作用。该疾病影响着大量患者,需要长期的训练治疗以及持续的社会支持,给社会和患者家庭带来了巨大的经济和伦理负担。临床上,PTSD患者往往对相对较小的刺激表现出过度的防御反应,表现出被激怒的行为,如何有效改善PTSD患者的过度防御行为是目前全世界急需解决的问题。
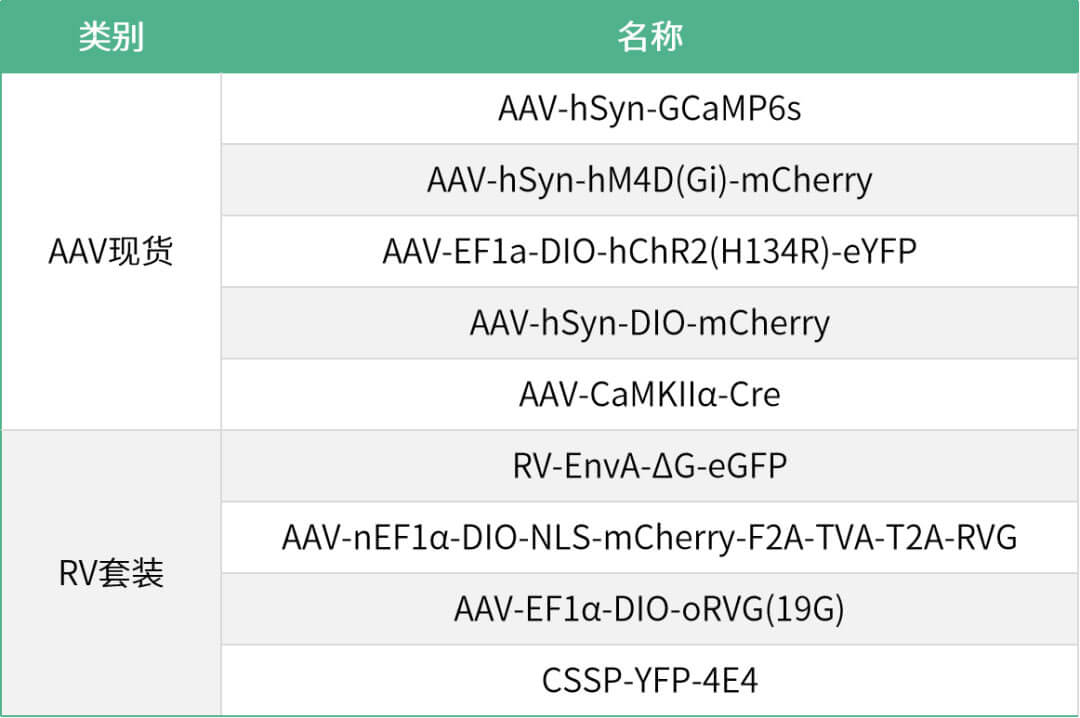
2023年2月3日,空军军医大学基础医学院武胜昔/郭保霖团队在Science Advances杂志上发表题为“Reversal of hyperactive higher-order thalamus attenuates defensiveness in a mouse model of PTSD”的研究成果。该研究团队利用SPS&S小鼠模型构建了一种可以有效拟合PTSD患者过度防御行为的PTSD模型小鼠,通过光遗传学及化学遗传学等多种调节方式,环路调节高阶丘脑的神经元活动,有效地改善了PTSD模型小鼠过度增强的防御行为。

研究者发现, PTSD模型小鼠存在过度的对于胡须刺激和创伤相关环境诱导的防御行为,在防御行为过程中,PTSD模型小鼠高阶丘脑-丘脑后内侧核(PoM)的神经元活动性显著升高,同时其抑制性的上游输入的来源脑区丘脑网状核(TRN)的神经元活动性降低,前联合皮层(FrA)为PoM的下游与防御相关的作用脑区。
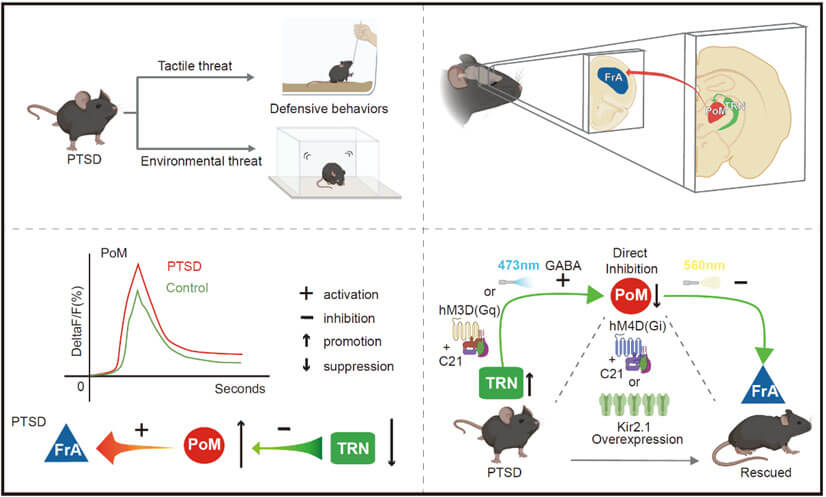
通过在PoM原位过表达内向整流钾离子通道Kir2.1或者化学遗传学抑制PoM的神经元活动性,可以有效改善PTSD模型小鼠过度增强的防御行为。同时,通过化学遗传学特异性地激活对PoM有投射的TRN神经元或者光遗传学激活TRN投射到PoM脑区的轴突终末,均可以有效改善PTSD模型小鼠的过度增强的防御行为。
并且,该研究通过狂犬病毒逆行示踪技术和Fos TRAP技术首次验证前联合皮层FrA为PoM下游与防御行为相关的作用脑区,通过光遗传学特异性地抑制PoM投射到FrA的轴突终末,可以有效改善PTSD模型小鼠的过度增强的防御行为。
据此,课题组在PTSD模型SPS&S小鼠上,实验证实了环路调节高阶丘脑可以有效地改善PTSD的过度防御行为,为潜在的临床靶向治疗提供了理论依据。
原文链接:https://www.science.org/doi/10.1126/sciadv.ade5987